تنظیم تعادل اکسیداسیون ـ احیا تیول برای پروسههای متابولیک، پیامرسانی و رونویسی چندگانه در سلولهای پستانداران بسیار مهم است. گروههای تیول، چه در پروتئینها و چه در مولکولهای کوچک، بسیار واکنشپذیر و حساس به اکسیداسیون هستند که میتواند باعث کاهش قابل توجه فعالیت بیولوژیکی شود. در پروتئینها، اکسیداسیون گروههای آزاد تیول باعث ایجاد تغییراتی میشود که بسته به موقعیت آنها ممکن است بر ساختار، فعالیت کاتالیزوری یا توانایی درگیر شدن در تعاملات پروتئینی تاثیر بگذارد. یک عملکرد حیاتی سیستمهای بافری اکسیداسیون احیا تيول بر پایه سلولی، حفاظت از گروههای تيول در مقابل گونهی فعال اکسيژن و ترمیم آنهاست که ممکن است به علت متابولیسم سلولی طبیعی یا غیر ضروری اکسید شوند. اجزای کلیدی سیستم بافری اکسیداسیون احیا تيول عبارتند از: سیستئین / سیستئین، جفت باز گلوتاتیون(GSH) / گلوتاتیون دی سولفید (GSSG) و اکسیدوردوکتازهای تیول_دی سولفید که شامل thioredoxin (Trx)، (Grx) glutaredoxins و پراکسیدوکسینها (Prx)هستند.
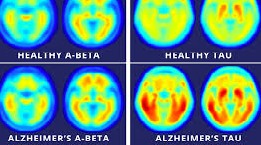
مطالعات زیادی انجام شده که توازن بازخوانی GSH را در اختلالات مغزی دخیل میدانند که موضوع بررسی چندین سال اخیر است؛ یکی از استدلالهای قانعکنندهای که برای شبکههای نظارتی تیول در بیماریهای نوروژنیک تولید میکند، شواهدی از بیان تغییر در بافتهای پس از مرگ یا در سلولهای سرطانی و پلاسما است. برای این منظور، نمونههای بعد از مرگ متابولیسم از بیماران مبتلا به دیابت بررسی شدهاست، که در آن مشاهده شد که محتوای گلوتاردوکسین در پارکینسون کاهش مییابد، به ویژه در نورونهای دوپامینرژیک که بیشتر نقش بازدارندگی در پارکینسون را پشتیبانی میکند. افزایش S-nitrosylation پروکسیردوکسین در مغز انسان مبتلا به پارکینسون، مانع هر دو فعالیت آنزیمی و عملکرد محافظتی آن از استرس اکسیداتیو میشود.
پیشرفتهای زیادی در درک اهمیت عدم تعادل بازتوانی تیول به عنوان عامل مهمی در بیماریهای نوروژنیک ایجاد شده است. واکنش پذیری بیولوژیکی اتم گوگرد در سیستئین، به عنوان یک اسید آزاد یا در پروتئینها و پپتیدها، عامل مهمی در تعیین حساسیت به آسیب اکسیداتیو، تحریک پذیری و تولید عصبی است. واضح است که بازسازی تعادل اکسیداسیون ـ احیا یک رویکرد مفید برای به حداقل رساندن زیانهای عصبی در طول تولید عصب میباشد. در بافت مغز پس از مرگ بیماران مبتلا به آلزایمر، بسیاری از رگهای خونی رنگآمیزی شده پروکسیردوکسین را نشان دادند که به علت فرآیندهای آستروستیک است. افزایش گلوتاردوکسین و کاهش ترشح نورونی تیوردوکسین در مغزهای بیماران مبتلا به آلزایمر دیده شده است. علاوه بر این، تغییرات اکسیداتیو در ۲ـپروکسیردوکسین و ۶ـپروکسیردوکسین در پلاسمای بیماران مبتلا به آلزایمر افزایش یافت.
منابع:
McBean, G.J., Aslan, M., Griffiths, H.R. and Torrão, R.C., 2015. Thiol redox homeostasis in neurodegenerative disease. Redox biology, 5, pp.186-194
Zhang, J., Zhang, Z., Zhang, W., Li, X., Wu, T., Li, T., Cai, M., Yu, Z., Xiang, J. and Cai, D., 2018. Jia-Jian-Di-Huang-Yin-Zi decoction exerts neuroprotective effects on dopaminergic neurons and their microenvironment. Scientific reports, 8.