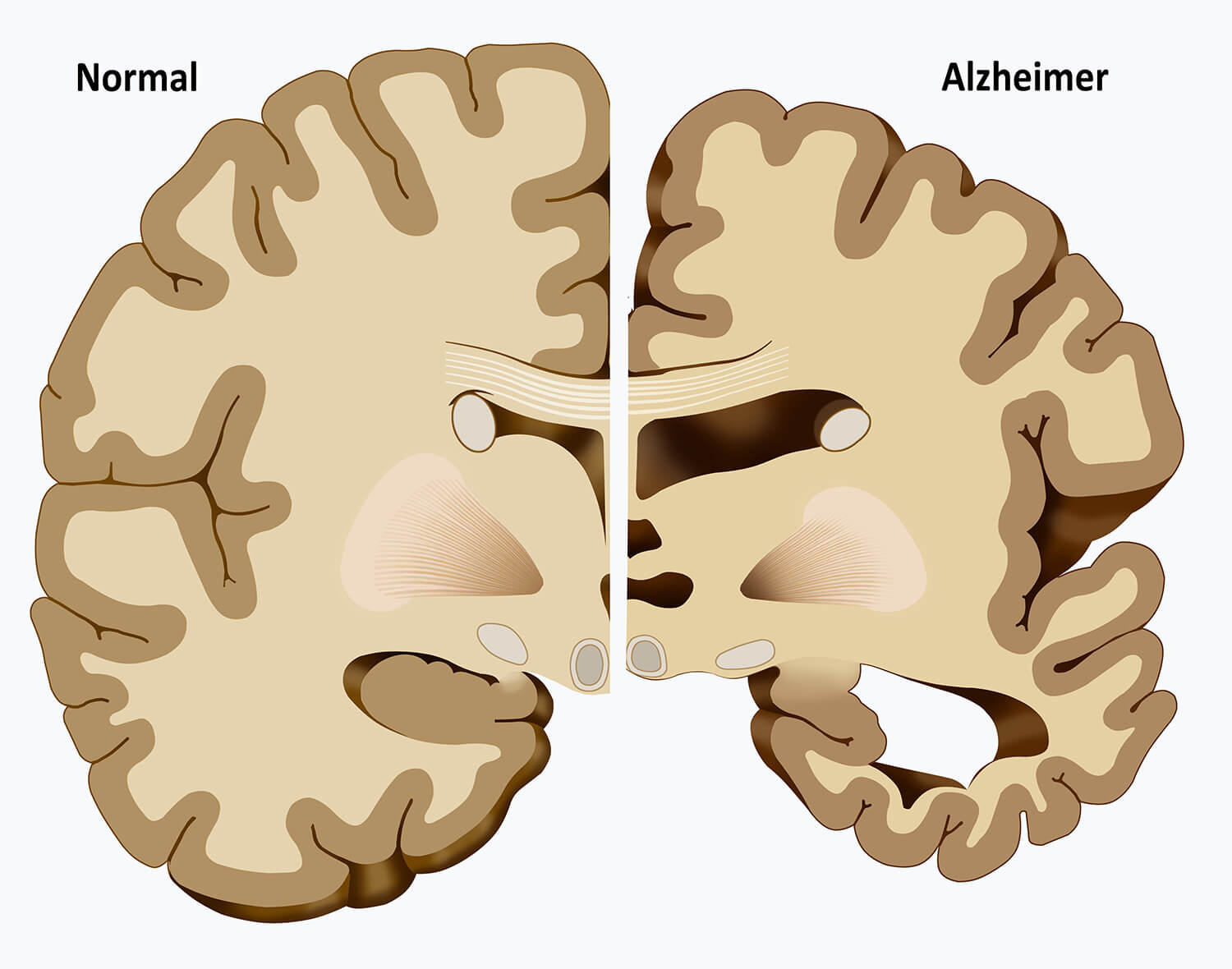
اکسیدنیتروژن، مولکول گازی تولید شده در مغز، میتواند به نورونها در زمان تولید اکسیدنیتریک بالا در مغز آسیب برساند که به شدت در پیشرفت سکته مغزی و ناهنجاریهایی مانند آلزایمر موثر است. محققان اخیرا کشف کردند که اکسیدنیتریک نه تنها باعث آسیب به نورون میشود، بلکه مکانیسمهای ترمیم مغز را نیز خاموش میکند.
در یک مطالعه، سرنخهای جدیدی در مورد اینکه چگونه واکنشهای شیمیایی طبیعی در مغز میتواند به آسیب مغزی و از دستدادن حافظه و عملکرد شناختی در برخی از بیماریها منجر شود، کشف کردهاند. این سرنخهای مولکولی جدید مهم هستند؛ چرا که ممکن است یک استراتژی جدید برای درمان سکته مغزی و اختلالات دیگر را توسعه دهند تنها اگر روش تاثیر عکس اکسیدنیتریک بر روی یک آنزیم خاص در سلولهای عصبی مشخص شود.
اکسیدنیتریک مسیر انتقال سیگنال ERK1 / 2 نوروپروتئینی را مهار میکند
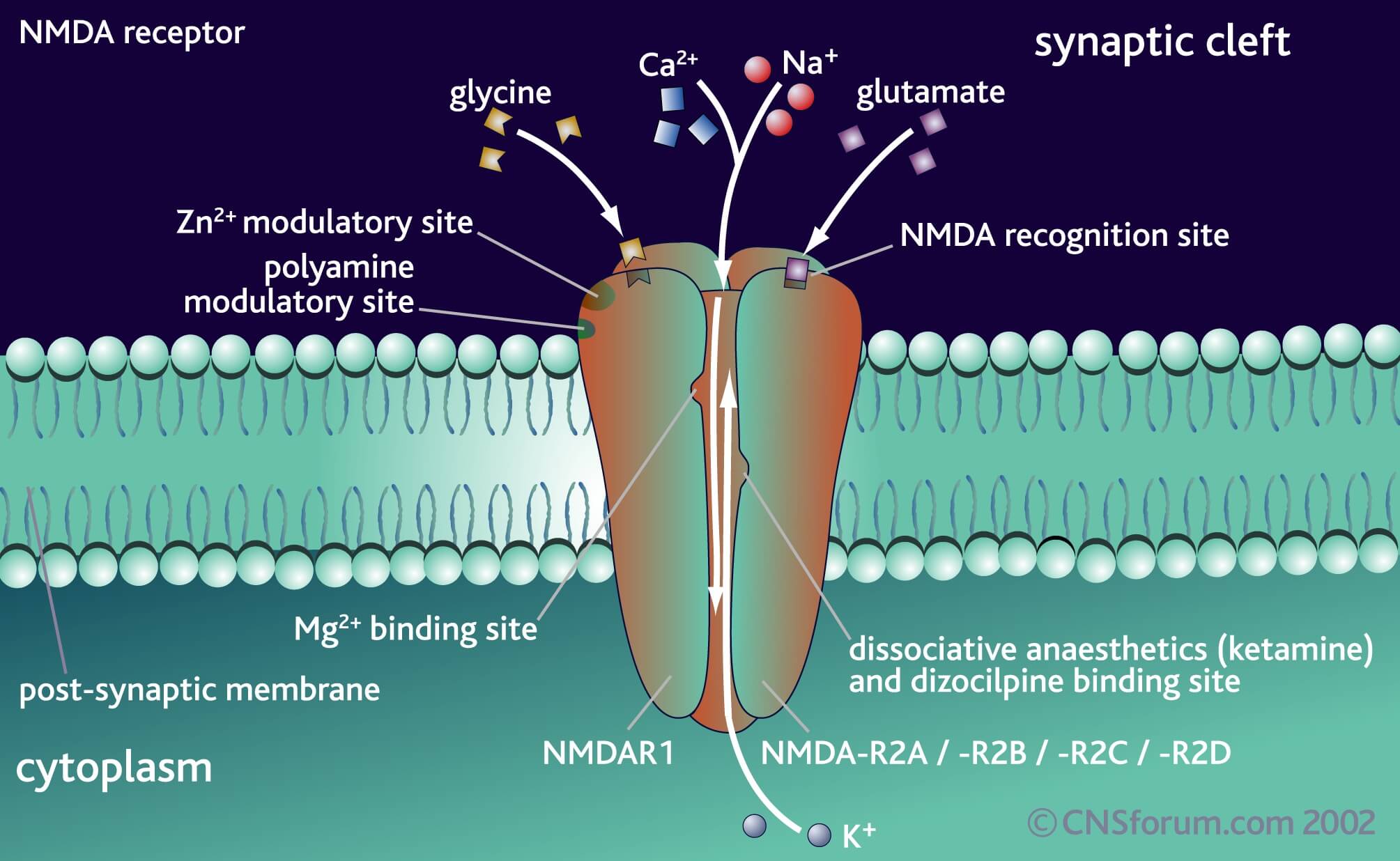
یادگیری و حافظه به طور جزئی توسط گیرندههای گلوتامات NMDA در مغز کنترل میشود. این گیرندهها با منافذ غشای سلول عصبی مرتبط هستند که جریان کلسیم و سدیم را در سلولهای عصبی و خارج از آن تنظیم میکنند. هنگامی که این گیرندههای NMDA بیش از حد فعال شوند، منجر به تولید اکسیدنیتریک شده و به نوبه خود، اکسیدنیتریک به وسیله یک واکنش به نام S-nitrosylation به پروتئینهای دیگر متصل میشود که اولین بار توسط لیپتون و همکارانش کشف شد. در حالیکه پروتئینهای S-nitrosyllated در بقای سلول و طول عمر سلول دخیل هستند، اکسید نیتریک میتواند سلولهای مغزی را از بین ببرد، که این مساله یکی از نشانههای بیماریهای عصبی است.
در آخرین مطالعه، محققان از نورونهای کشت شده و همچنین یک مدل موش سوری مبتلا به سکته مغزی استفاده کردند تا رابطه اکسیدنیتریک با پروتئینهایی که به آسیبهای عصبی کمک میکند، شناسایی کنند. آنها دریافتند که اکسید نیتریک با آنزیم SHP-2 واکنش داده تا رویدادهای مولکولی شناخته شده به عنوان مسیر سیگنال ERK1 / 2 را مهار کند. بنابراین، نیتریک اکسید نه تنها منجر به آسیب نورون میشود، بلکه توانایی مغز در خودترمیمی را نیز خاموش میکند.
منابع:
Khansari, N., Shakiba, Y. and Mahmoudi, M., 2009. Chronic inflammation and oxidative stress as a major cause of age-related diseases and cancer. Recent patents on inflammation & allergy drug discovery, 3(1), pp.73-80.
Gill, M.B. and Perez-Polo, J.R., 2008. Hypoxia ischemia-mediated cell death in neonatal rat brain. Neurochemical research, 33(12), pp.2379-2389.
Fukumura, D., Kashiwagi, S. and Jain, R.K., 2006. The role of nitric oxide in tumour progression. Nature Reviews Cancer, 6(7), p.521.