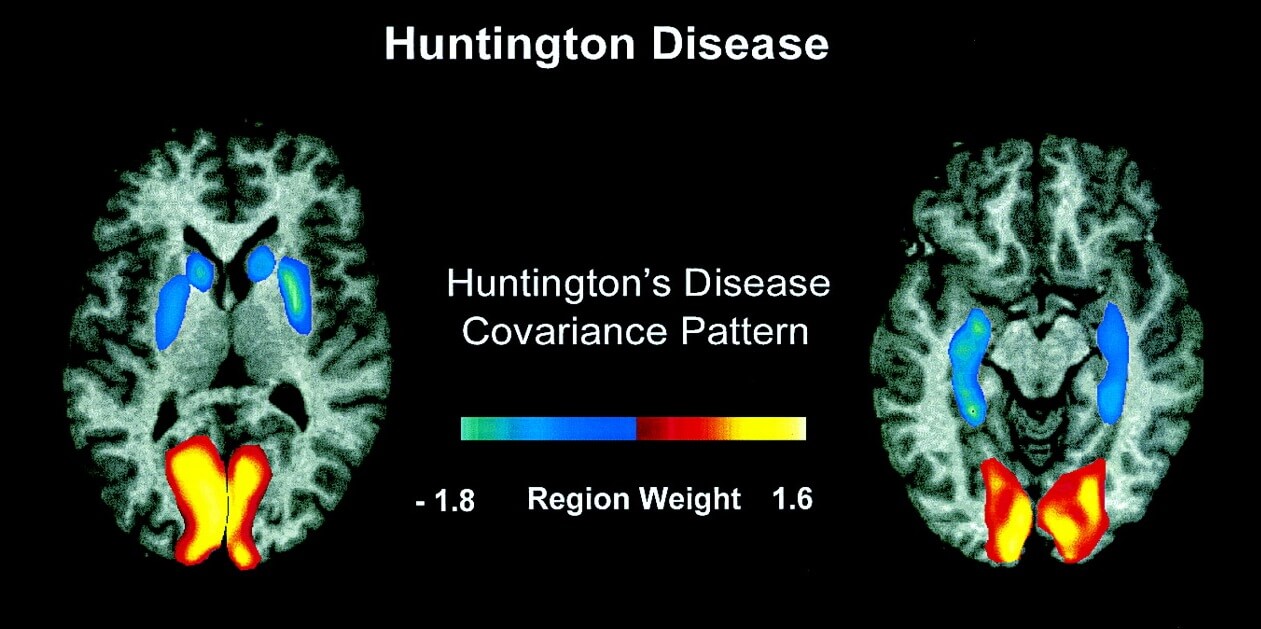
نوع خاصی از آسیب به نام “استرس اکسیداتیو” ممکن است به سلولهای بیمار و مرگ در بیماری هانتینگتون کمک کند. گزارشهای قبلی نشان میدهد که بیومارکر استرس اکسیداتیو میتواند به عنوان یک بیومارکر برای آزمایشات بالینی HD ( بیماری هانتینگتون) بررسی شود. اما به تازگی مطالعهای منتشر شده که نشان میدهد که این بیومارکر مفید محسوب نمیشود. آیا این خبر بد است؟
هدف اکثر مطالعات بر روی بیماری هانتینگتون، ایجاد درمان موثر برای بیماران است. برای رسیدن به این هدف ، باید صنعت دارو را در این زمینه گسترش داد و برای دریافت دارو، باید آزمایشهای بالینی صورت بگیرد تا اثر بخشی آنان مشخص گردد. اما چگونه میتوانیم بدانیم که درمان موثر است؟
درباره برخی داروها به راحتی میتوان اثربخشی آنان را تایید کرد زیرا به روشنی بر علایم HD تأثیر مثبتی دارند، همانند تاثیر بر حرکات فیزیکی مربوط به بیماری. اما ایدهآل محققین رسیدن به دارویی است که درواقع باعث جلوگیری، کند شدن و یا توقف ساخت سلولهای مغزی شود که باعث ایجاد HD میگردد. این مساله در بیماری هانتینگتون و سایر بیماریهای مغزی بسیار سخت است، زیرا نمیتوان به طور مستقیم مغز را بررسی و عملکرد دارو را سنجید. بیومارکر چیزی است که میتواند در مغز سنجیده شود و اطلاعاتی درباره اتفاقاتی که در مغز میافتد در اختیار قرار دهد.
بیومارکرها واقعا مهم هستند، زیرا آنها توانایی پیشرفت به سوی درمانهای موثر را دارند. محققان نیاز به سنجشهای قابل اعتماد و ساده دارند و اینکه بدانند در مغز بیماران هانتینگتون چه اتفاقی میافتد، بدون اینکه مجبور شوند جمجمهها را باز کنند. همچنین یک بیومارکر خوب میتواند در تعیین اینکه آیا یک داروی جدید دارای اثر مفید بر HD بوده یا نه مورد استفاده قرار بگیرد
استرس اکسیداتیو در HD
یکی از مواد تولیدشده توسط تمام سلولهای بدن، از جمله مغز، یک ماده شیمیایی به نام 8OhdG است. نام شیمیایی آن 8هیدروکسی دزوکسی گوانوزین بوده و تشخیص آن بسیار ساده است. سلولهای ما به طور مداوم در معرض انواع استرس هستند. یکی از مهمترین انواع استرسها، استرس اکسیداتیو نامیده میشود. اساسا ما به اکسیژن نیاز داریم تا نیاز به انرژی را تامین کنیم، اما اکسیژن مولکول مضر نیز میتواند باشد و 8OhdG یک ماده شیمیایی است که وقتی اکسیژن DNA را تخریب میکند، تولید میشود.
در سال 1997، دکتر فلینت بیال از کالج پزشکی Weil Cornell، سطوح بالای 8OhdG را در مغز افرادی که در اثر بیماری هانتینگتون جان خود را از دست داده بودند،نشان داد و این مطالعه در کارهای بعدی منجر به این ایده شده است که HD با افزایش استرس اکسیداتیو همراه است.
بر اساس این ایدهها در مورد افزایش استرس اکسیداتیو در بیماری هانتینگتون، در سال 2006 یک گروه تحت هدایت دیانا روسس و استیو هرش در بیمارستان عمومی ماساچوست در بوستون، میزان بیومارکر 8OhdG را در خون بیماران HD که تحت تیمار دارویی بودند، بررسی کردند . نتایج بسیار جالب توجه بودند، آنها دریافتند که بیماران HD دارای میزان بالاتری از 8OhdG نسبت به افراد کنترلشده هستند که در حقیقت، 8OhdG بیش از سه برابر که افزایش چشمگیری است محاسبه شد. دارویی که مورد آزمایش قرار گرفت، creatine نامیده شد که به نظر میرسید استرس اکسیداتیو را کاهش میدهد. در واقع، مصرف این دارو میزان 8OhdG را کاهش میدهد.
بر پایه نتایج این آزمایش نسبتا کوتاهمدت ، creatine بر روی حدود 650 بیمار مبتلا به HD، برای مدت طولانیتری تست شده است. این آزمایش جدید که CREST-E نامیده میشود، سطوح 8OhdG را در خون نیز اندازهگیری میکند.
8OhdG بیانگر چیست ؟
مطالعات اخیر نشان داده است که 8OhdG کاملا به همان اندازه که انتظار میرفت مفید نیست. به عنوان یک بیومارکر مفید، انتظار میرفت تغییرات سطوح آن در افراد قبل از ابتلای شدید به بیماری هانتینگتون مشاهده شود. در سال 2012 مطالعهای تحت عنوان PREDICT-HD ( پیشبینی بیماری هانتینگنون ) بر اساس بیومارکر 8OhdG انجام شد. این مطالعه علایم افراد مبتلا به جهش HD را بررسی میکند، اما هنوز نشانههایی از بیماری را نشان نمیدهند. اینها افرادی هستند که در آینده درمان خواهند شد و نتیجه بررسی تغییرات در این جمعیت، گامی مهم در جهت توسعه آزمایشهای دارویی مناسب است.
سطح 8OhdG در خون افراد در مطالعه PREDICT-HD اندازه گیری شد. در این گروه، تغییرات بسیار کمی در سطوح 8OhdG وجود دارد. تجزیه و تحلیل پیچیده ریاضی نشان داد که ممکن است افزایش سطح 8OhdG در افرادی که دارای جهش HD هستند، افزایش یابد، اما تغییر بسیار کم خواهد بود. محققان PREDICT-HD با استفاده از دو تکنولوژی متفاوت برای اندازهگیری 8OhdG به نتایج متضاد رسیدند که یکی از آنها بیانگر افزایش اندک و دیگری هیچ تغییری را نشان نداد.
مطالعات جدید در جهت بررسی اهمیت 8OhdG
این مطالعات گیجکننده بودند و دانستن اینکه آیا 8OhdG میتواند در بیماران HD به عنوان یک بیومارکر اندازهگیری شود یا نه را دشوار میکرد. به امید روشن شدن این مسئله، دانشمندان بنیاد CHDI و TRACK-HD مطالعه جدیدی را انجام دادند که به طور اختصاصی در مورد درک آنچه برای8OhdG در خون بیماران HD و حاملهای جهش اتفاق میافتد، طراحی شده است. در ابتدا این دانشمندان به دقت تکنولوژی اندازه گیری این بیومارکر را بررسی کردند، زیرا بدون اندازهگیری دقیق، هیچ نتیجهای نمیتواند مورد استفاده قرار بگیرد.
با درک روشنی از دقیق بودن ابزارهای سنجش، تیم به 320 نمونه خون تحت مطالعه TRACK-HD تقسیم شد. این مطالعه به دقت افرادی که دارای جهش HD هستند را بررسی میکند. با استفاده از هر دو روش اندازهگیری، این مطالعه دقیق به وضوح ثابت میکند که در خون افراد مبتلا به جهش HD اختلاف سطح 8OhdG وجود ندارد. سطح بیومارکر در ابتدا و با پیشرفت بیماری تغییری نکرد. این بدان معنی است که سطوح 8OhdG یک نشانگر خوب برای آزمایشات HD نیست.
این ممکن است بد به نظر برسد، در ابتدا تصور میشد 8OhdG ممکن است یک بیومارکر خوب برای تیمارهای دارویی HD باشد، و اکنون مشخص شده است که اینگونه نیست. اما در واقع این اطلاعات بسیار مفید است. دانستن اینکه 8OhdG مفید نیست، محققان را قادر میسازد که بر روی بیومارکرهای جدیدی که میتواند در این بیماری مورد سنجش قرار بگیرند، تمرکز کنند.
مطالعاتی مانند PREDICT-HD و TRACK-HD مجموعه عظیمی از بیومارکرهای بالقوه احتمالی برای پیگیری در اختیار قرار دادهاند و این بدان معنی است که محققان یک گام به یافتن بیومارکر مفید در HD نزدیک شدهاند.
منابع:
Rosas, H.D., Lee, S.Y., Bender, A.C., Zaleta, A.K., Vangel, M., Yu, P., Fischl, B., Pappu, V., Onorato, C., Cha, J.H. and Salat, D.H., 2010. Altered white matter microstructure in the corpus callosum in Huntington’s disease: implications for cortical “disconnection”. Neuroimage, 49(4), pp.2995-3004.
Lerch, J.P., Carroll, J.B., Dorr, A., Spring, S., Evans, A.C., Hayden, M.R., Sled, J.G. and Henkelman, R.M., 2008. Cortical thickness measured from MRI in the YAC128 mouse model of Huntington’s disease. Neuroimage, 41(2), pp.243-251.
Biglan, K.M., Ross, C.A., Langbehn, D.R., Aylward, E.H., Stout, J.C., Queller, S., Carlozzi, N.E., Duff, K., Beglinger, L.J. and Paulsen, J.S., 2009. Motor abnormalities in premanifest persons with Huntington’s disease: The PREDICT‐HD study. Movement Disorders, 24(12), pp.1763-1772.
Georgiou-Karistianis, N., Hannan, A.J. and Egan, G.F., 2008. Magnetic resonance imaging as an approach towards identifying neuropathological biomarkers for Huntington’s disease. Brain research reviews, 58(1), pp.209-225.