کاهش مقادیر آنزیم کاتالاز سلولهای سرطانی را در مقابل دوز بالای ویتامین C آسیبپذیر میکند.
ویتامین C تاریخچه منقطعی در درمان سرطان دارد اما محققین دانشگاه آیُوا (UI) بر این باورند که راه درست استفاده از این ماده پیش گرفته نشده است.
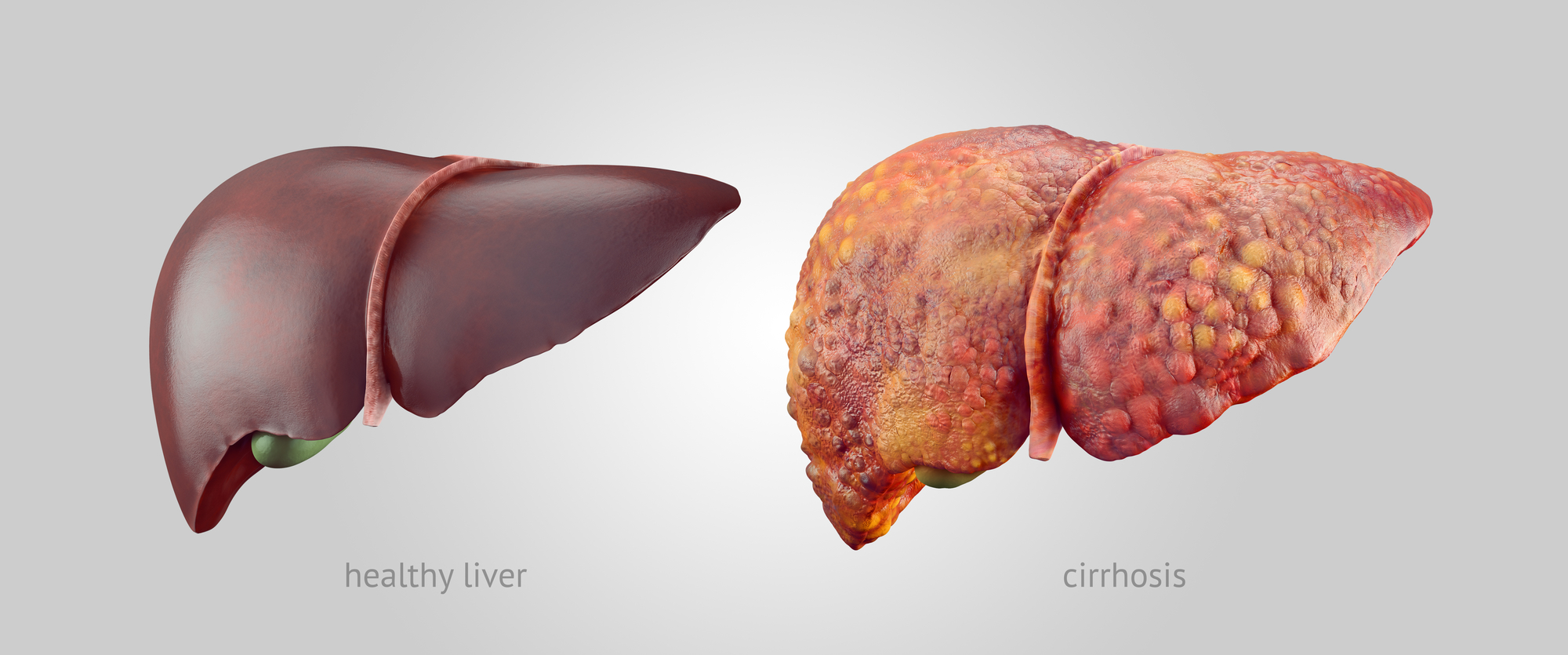
بسیاری از درمانهای مبتنی بر ویتامین C بر دریافت دهانی این ماده استوارند. با این وجود دانشمندان UI نشان دادهاند که تجویز این ماده بهصورت داخل وریدی با حذف متابولیسمهای کبدی و مسیرهای دفعی سطوحی ۱۰۰ تا ۵۰۰ برابر تجویز دهانی در بدن ایجاد میکند. این سطوح به مقادیر بسیار بالای ویتامین C که برای حمله به سلولهای سرطانی مورد نیاز است، بسیار نزدیک است.
پیشتر گفته بودیم که آنتی اکسیدانتها باعث تسریع پیشرفت سرطان ریه می شوند اما، مطالعات قبلی گری بوتنر، متخصص زیستشناسی ردوکس این دانشگاه نشان داده است که در این مقادیر بالا (در حدود میلیمولار) ویتامین C بهصورت انتخابی فقط سلولهای سرطانی را مورد هدف قرار داده و از بین میبرند. این شرایط در موشها و شرایط آزمایشگاهی مورد تایید قرار گرفته است. پزشکان بیمارستان و کلینیک UI اکنون در حال آزمایش این رویکرد (تجویز وریدی دوز بالای ویتامین C) در بیماران مبتلا به سرطان پانکراس و ریه بهصورت همزمان با شیمیدرمانی و رادیوتراپی، هستند. آزمایشهای بالینی فاز یک قبلا امنیت و کم خطر بودن این درمان را تایید کردهاند و در آزمایشهای بعدی هدف بررسی اثرات این درمان در افزایش نرخ زندهمانی خواهد بود.
در مطالعه جدیدی از این تیم که اخیرا در مجله Redox Biology چاپ شده محققین به بررسی جزئیات بیشتری از نحوه تاثیر ویتامین C (آسکوربات) بر سلولهای سرطانی پرداختهاند. این مطالعه نشان میدهد که ویتامین C بهسرعت به هیدروژن پراکسید شکسته می شود و گونههای فعال اکسیژن تولید میکند. سلولهای سرطانی بسیار حساس به صدمه در مقابل غلظت بالای هیدروژن پراکسید هستند.
سلولهای طبیعی راههای متفاوتی برای حذف هیدروژن پراکسید دارند و مقادیر آنرا در حد بسیار پایین نگه میدارند. در نتیجه آسیبی به این سلولها وارد نمیشود. مطالعات جدید نشان میدهد که آنزیم کاتالاز نقش بسیار حیاتی در حذف هیدروژن پراکسید اضافی را دارد. محققین کشف کردهاند که سلولها با مقادیر کمتری از کاتالاز در هنگام رویارویی با غلظتهای بالای ویتامین C، نسبت به آسیب توسط هیدروژن پراکسید بسیار حساسترند.
نویسنده مسئول این مقاله عنوان میکند: نتایج ما نشان میدهد که سرطانهایی که باعث کاهش مقادیر آنزیم کاتالاز در سلول میشوند در مقابل این درمان حساستر بوده و سایر سرطانها نسبت به این درمان مقاومترند.
منبع:
Doskey, C.M., Buranasudja, V., Wagner, B.A., Wilkes, J.G., Du, J., Cullen, J.J. and Buettner, G.R., 2016. Tumor cells have decreased ability to metabolize H 2 O 2: Implications for pharmacological ascorbate in cancer therapy. Redox Biology, 10, pp.274-284.