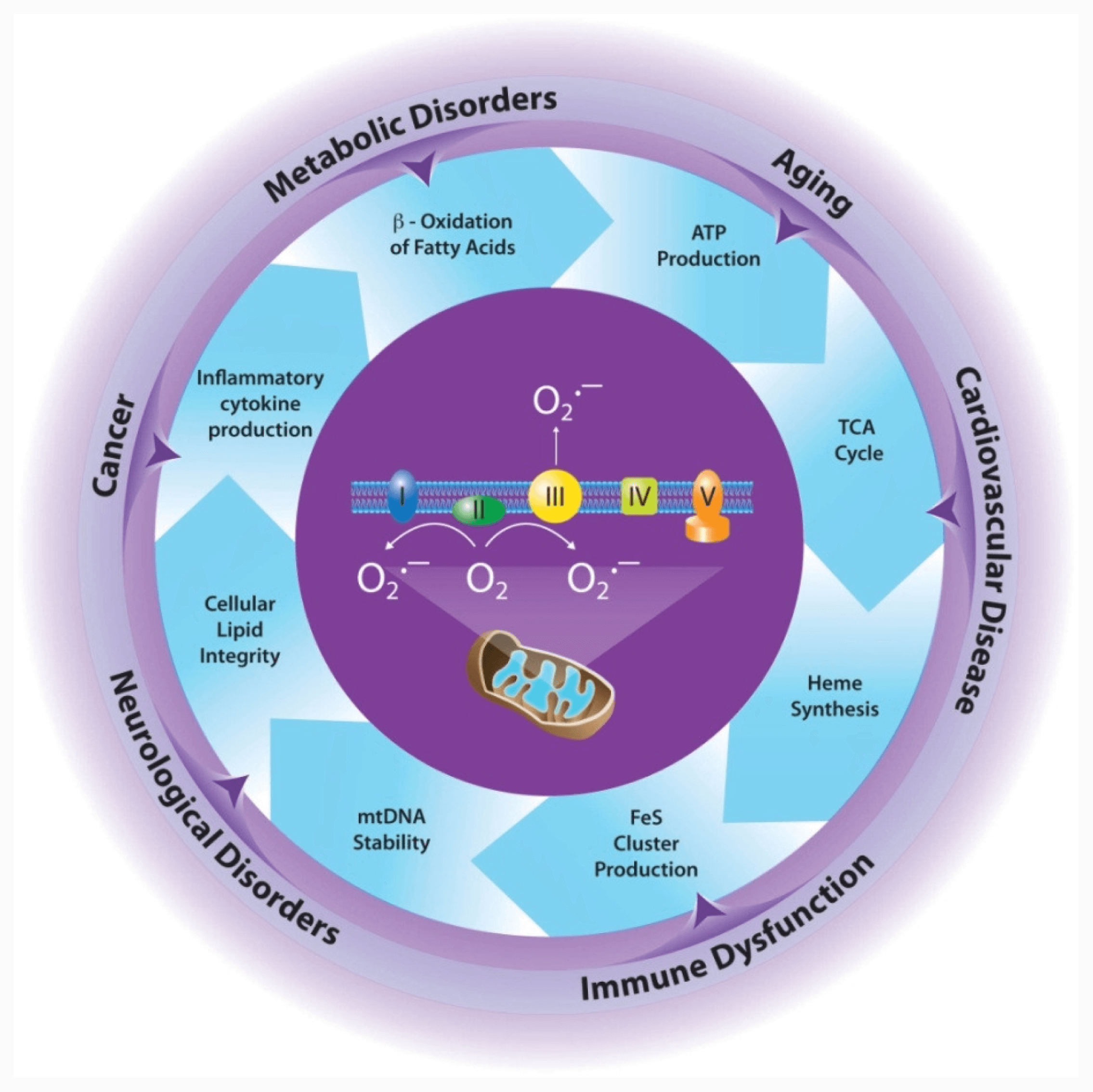
سوپراکسید دیسموتاز (SOD)آنزیمی است که سلولها را تعمیر میکند و باعث تخریب سوپراکسید، شایعترین رادیکال آزاد در بدن میشود. این آنزیم در هر دو درم و اپیدرم وجود دارد و کلید تولید فیبروبلاستهای سالم (سلولهای ساختمانی پوست) میباشد.
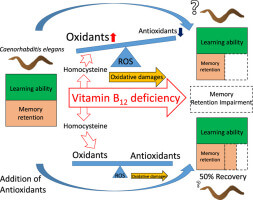
مطالعات نشان دادهاند که SOD به عنوان آنتیاکسیدان و ضد التهاب در بدن عمل کرده و باعث خنثیسازی رادیکالهای آزاد میشود و میتواند از پیری و تغییرات سلول پیش سرطانی جلوگیری کند. محققان در حال مطالعه پتانسیل سوپراکسید دیسموتاز به عنوان یک درمان ضد پیری هستند، زیرا هماکنون مشخص شده است که با افرایش سن میزان SOD کاهش و مقدار رادیکالهای آزاد افزایش مییابد.
سوپراکسید دیسموتاز به بدن در استفاده از روی، مس و منگنز کمک میکند. دو نوع SOD وجود دارد: سوپراکسید دیسموتاز مس / روی (Cu / Zn) و سوپراکسید دیسموتاز منگنز (Mn) . هر کدام نقش متفاوتی در حفظ سلولهای سالم دارند به عنوان مثال Cu / Zn SOD از سیتوپلاسم سلولی و Mn SOD از میتوکندریهای سلولی در برابر آسیب رادیکالهای آزاد محافظت میکند.
اختلال در ژن سوپراکسید دیسموتاز وابسته به مس و روی میتواند در بعضی از افراد باعث ایجاد بیماری اسکلروز جانبی آمیوتروپیک (ALS) یا Lou Gehrig میشود. ALS یک بیماری کشنده است که سبب تحلیل سلولهای عصبی در مغز و نخاع میشود. نظریه این است که سطوح پایین سوپراکسید دیسموتاز در سلولهای عصبی منجر به آسیب از طریق رادیکال آزاد و مرگ سلولی میشود. در این راستا محققان تأثیر ویتامین E و دیگر مکملهای آنتیاکسیدانی را نیز در پیشرفت این بیماری مطالعه کردهاند.
مطالعات اولیه امیدوار کننده بوده و نشان داد که مکملهای ویتامین E میتواند پیشرفت ALS را کند کند، برخی محققان ادعا میکنند که خطر ابتلا به ALS در افراد دارای رژیم غذایی ویتامین E در مقایسه با افراد بدون رژیم ویتامین E ، شصت و دو درصد کمتر است.
سوپراکسید دیسموتاز همچنین برای درمان آرتریت، مشکلات پروستات، زخم قرنیه، سوختگی، بیماریهای التهابی، بیماری التهابی روده و آسیبهای دراز مدت حاصل از قرار گرفتن در معرض دود و اشعه و برای جلوگیری از عوارض جانبی داروهای سرطانی استفاده شده است. در شکل مصرف موضعی آن ممکن است به کاهش چین و چروک صورت، بافت زخم، سوختگیها و تیرگی پوست کمک کند و از اشعههای مضر UV محافظت نماید.
SOD در جو، بروکلی، کلم، گندم و بیشتر گیاهان سبز یافت میشود. بدن به مقدار زیادی ویتامین C و مس نیاز دارد تا این آنتیاکسیدان طبیعی را تولید کند بنابراین باید این مواد از طریق رژیم غذایی تامین شود. همچنین SOD میتواند به وسیله تزریق، مکملهای خوراکی زیرزبانی، قرصها و کرمهای موضعی تامین شود. با این حال، در نظر داشته باشید که این ماده باید در روده کوچک جذب شود، بنابراین مهم است که مکملهای خوراکی را انتخاب کنید که به صورت پوشش روغنی یا زیر زبانی مصرف شوند. این عمل به منظور جلوگیری از تاثیر اسید معده جهت نابودی SOD قبل از جذب توسط روده کوچک ضروری است.
منابع:
Castagliuolo, I., Brun, P., Busiello, I. and Miraglia, N., Gnosis SpA, 2017. Formulations containing Saccharomyces boulardii and superoxide dismutase (SOD) to control obesity. U.S. Patent 9,555,082.
Zhao, H., Li, W., Zhao, X., Li, X., Yang, D., Ren, H. and Zhou, Y., 2017. Cu/Zn superoxide dismutase (SOD) and catalase (CAT) response to crude oil exposure in the polychaete Perinereis aibuhitensis. Environmental Science and Pollution Research, 24(1), pp.616-627.
Azadmanesh, J. and Borgstahl, G.E., 2018. A Review of the Catalytic Mechanism of Human Manganese Superoxide Dismutase. Antioxidants, 7(2), p.25.