در بسیاری از موارد RNA پیامبر یا mRNA میتواند ماشینهای سلولی تولیدکننده پروتئین را از کار بیاندازد. مشکل در تصفیه این ماشینهای سلولی از کار افتاده و mRNAهای ناکارآمد است که موجب بیماریهای نورودژنراتیوی چون آلزایمر میشود.
آسیب به DNA تقریبا موردی است که تمامی سلولها با آن مواجه هستند. این آسیب بیشتر در سرطان نمود پیدا میکند، چرا که مکانیسمهای ترمیمکننده این آسیبها از کار میافتند. موادی که باعث آسیب به DNA میشوند، میتوانند مولکول خواهر همان DNA که mRNA است را نیز تخریب کنند. وظیفه mRNA انتقال رونوشتهای ژن به هزاران ریبوزوم در هر سلول است، اما به تخریب در این ابعاد توجه بسیاری کمی شده است.
یکی از نشانههای بیماری آلزایمر استرس اکسیداتیو است و مطالعات نشان دادهاند که در بیماران مبتلا به آلزایمر پیشرفته، نیمی از مولکولهای RNA در سلولهای عصبی اکسیده شدهاند.
ظاهر، سیمز و همکاران در مطالعهای که اخیرا چاپ شده است عنوان کردهاند که وقتی mRNA اکسید شده را در مجاورت ریبوزوم قرار میدهند، ریبوزومها تخریب شده و از کار میافتند.
یک ریبوزوم معیوب (Stuck Ribosome) میتواند با فاکتورهایی که آنرا از mRNA جدا میکند و بخش معیوب mRNA را میجود، احیا شود اما در صورتی که این سیستم کنترل کیفیت وجود نداشته باشد، مولکولهای mRNA آسیب دیده در سلول تجمع پیدا میکنند. دقیقا همانند آنچه در بیماری آلزایمر شاهد آن هستیم.
مواردی وجود دارد که mRNA به اندازه DNA در رخداد یک بیماری دخالت داشته باشند. بوضوح آسیب اکسیداتیو به RNA در بسیاری از بیماریهای نورودژنراتیو دخیل است. درست است که عامل اصلی ایجاد بیماری RNA نیست اما در خلل این مسیر پاتولوژیک تولید شده و بعنوان یک محصول فرعی تاثیرگذار است. در حالت عادی فقط حدود یک درصد از کل mRNAهای سلولی اکسید شدهاند، اما در شرایط استرس اکسیداتیو، به هر دلیلی که ایجاد شده باشند، درصد بالای از mRNAها تخریب میشوند.
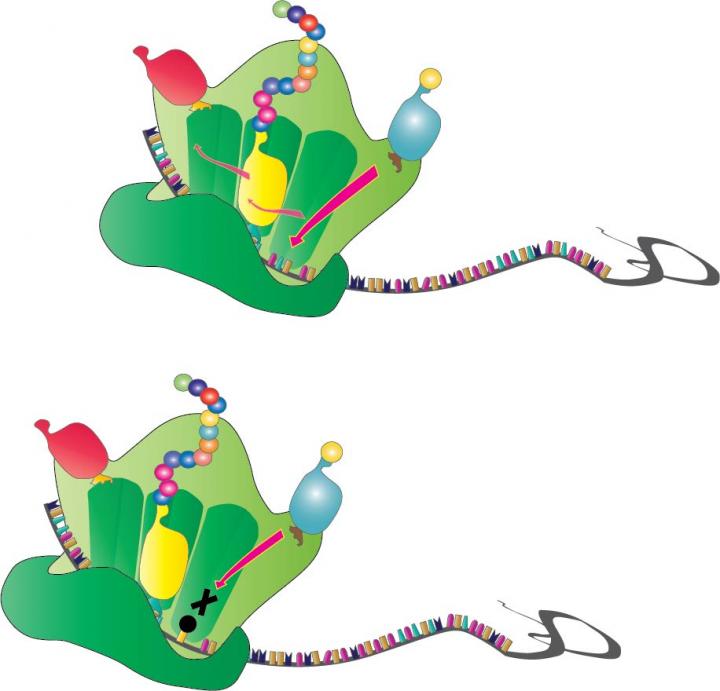
برای سنجش صحت و استحکام ترجمه، نویسندگان این مقاله mRNA آسیب دیده به ریبوزومها معرفی کردند. آنها یکی از حروف در واحدهای سه حرفی mRNA را تخریب کردند و با اکسیده کرده باز گوانین G محصولی تحت عنوان 8-oxo-G تولید کردند. چرا که یک باز G اکسید شده در زمان رونوشت برداری باعث یک خطا میشود و بجای جفت شدن با باز C، با باز A جفت میشود. در حقیقت بجای اینکه ریبوزوم توالی DNA مورد نظر که بصورت C[8-oxo-G]C است را بصورت CAC میخواند و با قرار دادن اسیدآمینه اشتباه، زنجیره پروتئین اشتباه تولید میکند.
نقطه شگفتانگیز این مطالعه اینجاست که انتظار میرفت با تفاسیری که شد، هنگامی که mRNA معیوب در مجاورت ریبوزوم قرار گیرد، محصول اشتباه تولید شود اما برخلاف انتظار ریبوزوم از کار باز ایستاد و نتوانست تعاملی با mRNA معیوب برقرار کند. برای جلوگیری از هرگونه شک و شبهه، دانشمندان هر یک از ۳ جایگاه کدون را با این ترکیب معیوب جایگزین کردند و هربار ریبوزوم واکنش یکسان نشان داده و از کار ایستاد.
چنین سیستم محافظتکننده نشان میدهد که وجود عیوب در mRNA تنها دلیل بر تجمع پلیپپتیدهای ناقص در داخل سلول نیست و احتمالا مشکلی در سیستمهای کنترل کیفی نیز بوجود میآید.
منبع:
Simms CL, Hudson BH, Mosior JW, Rangwala AS, Zaher HS. An active role for the ribosome in determining the fate of oxidized mRNA. Cell reports. 2014 Nov 20;9(4):1256-64.

