دانشمندان دانشگاه روتگرز پروتئینی را شناسایی کردند که باعث آسیب آنتیاکسیدانت و بیماریهای بسیاری است.
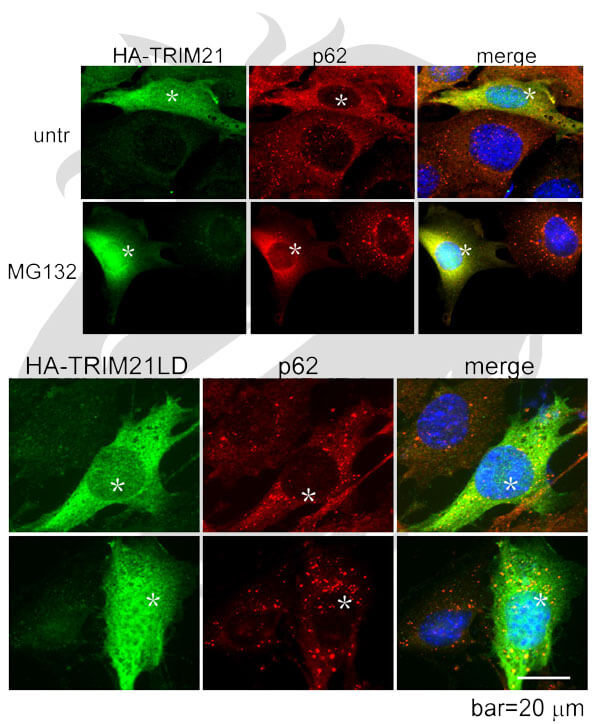
بر اساس مطالعه جدید چاپ شده در Molecular cell، دانشمندان دریافتند که پروتئینی تحت عنوان P62 که در حالت عادی میبایست بهعنوان یک آنتیاکسیدانت در جهت جلوگیری از صدمه سلولی عمل کند، در موشهای آزمایشگاهی مبتلا به بیماریهای قلبی و کبدی عملکرد مناسبی ندارد.
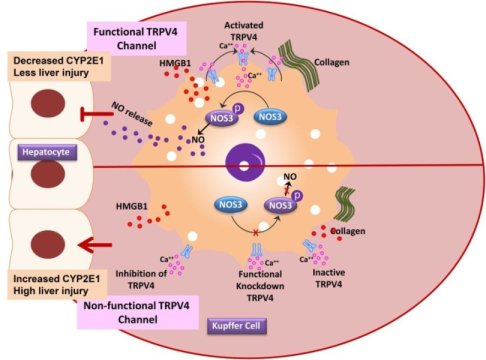
این امر باعث ایجاد استرس اکسیداتیو میشود و در نتیجه آن مولکولهای مضر در بدن آزاد میشود که آنها را رادیکالهای آزاد مینامند. سیستم آنتیاکسیدانتی سلولهای بدن به عنوان یکی از اولین سپرهای دفاعی بدن، میبایست از حمله این مولکولهای مضر دفاع کند و از صدمه دیدن سایر سلولها جلوگیری کند. پیشتر نیز در خصوص محافظت کبد در مقابل استرس اکسیداتیو مطلبی منتشر شده بود
دکتر وی-ژینگ-زونگ، رهبر این تیم تحقیقاتی میگوید: «علت این آسیب عملکرد عکس پروتئین دیگری بهنام TRIM21 است که میبایست سیستم ایمنی بدن را علیه باکتری و ویروس تحریک کند اما در این موشهای بیمار کاملا برعکس عمل کرده و باعث خاموش شدن پروتئین آنتیاکسیدانت شده و مانع از عملکرد آن میشود.
رهبر این تیم تحقیقاتی همچنین میافزاید:«پروتئین TRIM21 در حالت نرمال در بدن وجود دارد و بدون آن بدن ما در مقابل بسیاری از عفونتهای قابل کنترل مغلوب خواهد شد. اما این تحقیق به ما نشان میدهد که در شرایطی که بدن دچار روندهای پاتولوژیکی همزمان میشود، بهتر است که پروتئين TRIM21 را مهار کنیم چرا که مانع از حفاظت سلول در مقابل آسیب میشود.»
در این مطالعه دانشمندان با بررسی آسیبهای قلبی و کبدی در موشهای آزمایشگاهی دریافتند که در موشهایی که ژن TRIM21 غیرفعال شده داشتند در مقایسه با موشهای دارای ژن و در شرایط بیماریهای قلبی و کبدی، آسیب کمتری را متحمل شدهاند.
دکتر زونگ عنوان میکند: «قلب و کلیه در موشهای فاقد ژن TRIM21 در مقایسه با موشهای گروه شم بهنحو مناسبی محافظت شدهاند. این دادهها به ما کمک میکند تا شرایط مشابه را در انسان بهتر مدیریت کنیم.»
بیماریهای قلبی یکی از اصلیترین دلایل مرگومیر در ایالات متحده آمریکاست و این درحالی است که ۱۰٪ آمریکاییها به یکی از انواع بیماریهای کبدی مبتلا هستند. جالب است بدانید بر اساس اعلام رئیس انجمن قلب ایران شیوع مرگومیر ناشی از بیماریهای قلبی در ایران بالاتر از آمارهای جهانی است.
این تیم تحقیقاتی امیدوار است با طراحی و توسعه داروهای مناسب، فعالیت این پروتئین کاهش یا متوقف شود تا بتوان از بروز آسیبهای اشاره شده جلوگیری نمود.
منبع:
Pan J-A, Sun Y, Jiang Y-P, et al. TRIM21 ubiquitylates SQSTM1/p62 and suppresses protein sequestration to regulate redox homeostasis. Molecular cell. 2016;61(5):720-733. doi:10.1016/j.molcel.2016.02.007.