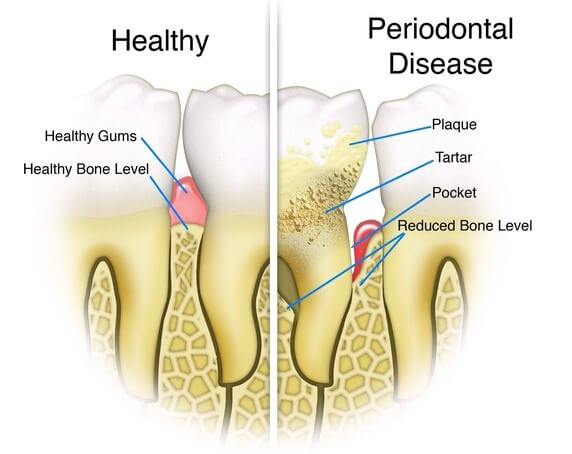
التهاب لثه (پریودنتال) باعث افزایش استرسهای اکسیداتیو شده و تولید گونههای اکسیداتیو فعال (ROS) در ادامه باعث آسیب بافتی میشود. همانطور که پیشتر گفته شد توسط مکانیسمهای مختلفی تولید میشوند. از آنجا که تولید ROS اجتناب ناپذیر است، لذا باید سیستم پیچیده از آنتی اکسیدانتها در دفاع در برابر استرس اکسیداتیو وجود داشته باشد. آنتی اکسیدانتهای تولید شده در بدن در کنترل اثرات و جلوگیری از آسیبهای ایجاد شده توسط گونه فعال کنترل نشده، مفید هستند.
ملاتونین (N استیل-5-متوکسی تریپتامین) هورمونی است که توسط غدد صنوبری و تا حدی نیز توسط شبکیه چشم، جسم مژگانی، لنز، غده اشکی، روده و پوست ترشح میشود و از طریق پلاسما به بزاق منتقل میشود. ملاتونین نسبت به سایر آنتی اکسیدانتها قویتر بوده و در هر دو سطح آنزیمی و ژنومی عمل میکند.ملاتونین به عنوان تنظیمکننده بیان ژنهای گلوتاتیون پراکسیداز و سوپراکسید دیسموتاز و همچنین یک مدولاتور ایمنی بدن و پروموتور تشکیل استخوان، شناخته شده است.
به منظور بررسی و مقایسه ظرفیت آنتیاکسیدانتی تام (TAC) و سطح هورمون ملاتونین در بزاق زنان مبتلا التهاب لثه مطالعهای در سال 2016 طراحی شد که در آن از دو گروه از زنان در گروه های سنی باروری و پس از یائسگی استفاده کردند زیرا سطح هورمون ملاتونین در یائسگی تغییر می کند.
مقادیر TAC، در زنان مبتلا به پریودنتیت مزمن به طور قابل توجهی کاهش مییابد. مطالعه بیشتر در مورد کاهش در سطح ملاتونین و ظرفیت تام آنتیاکسیدانتی (TAC) در زنان مبتلا به پریودنتیت مزمن نسبت افراد سالم ملاتونین نشان داد که ملاتونین بزاقی میتواند به عنوان یکی از نشانگرهای بیماری پریودنتال استفاده شود. با این حال مطالعات بیشتری در این زمینه نیاز هست تا بدانیم چگونه ملاتونین به عنوان یک آنتی اکسیدانت قوی عمل در دندان عمل می کند.
منبع:
Ramesh A, Prakash AP, Thomas B, Shetty M. Salivary melatonin and total antioxidant capacity in reproductive and postmenopausal women. Journal of the International Clinical Dental Research Organization. 2016 Jan 1;8(1):39.