- یک مطالعه برجسته که توسط محققان دانشگاه بلگراد صربستان انجام شده پیشنهاد کرده است که درمان آنتیاکسیدانی قادر به کاهش علائم بیماری سلیاک میباشد.
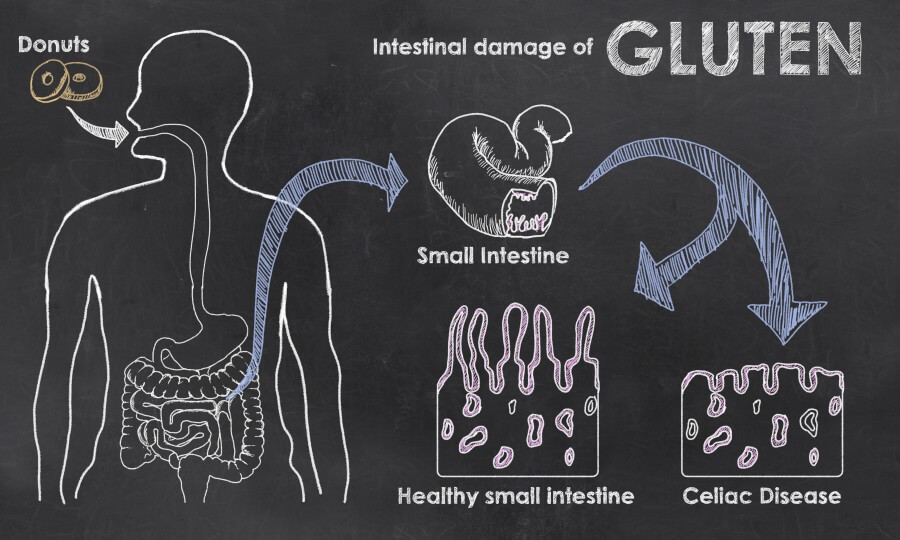
بیماری سلیاک یک بیماری جدی و غیر قابل درمان است که تقریبا 1 درصد کودکان و 1.2 درصد بزرگسالان را تحت تاثیر قرار میدهند. افراد مبتلا به بیماری سلیاک، از واکنشهای شدید و خطرناک گوارشی نسبت به گلوتن، پروتئین اصلی موجود در گندم و بسیاری از دانههای دیگر رنج میبرند. به طورکلی فعال شدن سیستم ایمنی توسط پپتیدهای گلوتن مسئول پاتوژنز و پیشرفت بیماری سلیاک است. گلوتن توازن آنتیاکسیدانی را در مخاط روده، احتمالا از طریق تولید بیش از حد رادیکالهای آزاد به هم میزند.
محققان، بیوپسی رودهای را در 39 کودک مبتلا به بیماری سلیاک فعال یا خاموش و در 19 فرد سالم با سن معادل انجام دادند تا این ارتباط را بین بیماری سلیاک، رادیکالهای آزاد و آنتیاکسیدانها بررسی کنند. محققان دریافتند که کودکان مبتلا به هر دو نوع بیماری سلیاک به طور قابل توجهی دارای سطوح آنتیاکسیدان معروف گلوتاتیون پایینتری هستند، در حالی که بیومارکر فعالیت آنتیاکسیدانی به طور معنیداری بیشتر است.
سطوح پایین مشاهده شده گلوتاتیون قابل توجه است، زیرا این ماده شیمیایی اغلب به عنوان آنتیاکسیدان اصلی شناخته میشود که مسئول اعطای الکترون به دیگر آنتیاکسیدانها میباشد تا توانایی مبارزه با رادیکال آزاد را افزایش دهد. یافتههای بیوشیمی بالینی نشان میدهد که در بیماران مبتلا به سلیاک، گلوتن ممکن است موجب سیل رادیکالهای آزاد در روده شود. این سیل چنان شدید است که به طور کامل ذخایر گلوتاتیون بدن را از بین میبرد، در نتیجه اثربخشی همه آنتیاکسیدانهای دیگر بدن را کاهش داده و منجر به افزایش آسیب اکسیداتیو و استرس در دستگاه گوارش میگردد. این نشان میدهد که رژیم غذایی با میزان آنتیاکسیدانها میتواند به کاهش شدت علائم سلیاک کمک کند.
استرس اکسیداتیو عامل مهمی در پاتوژنز بیماری سلیاک است. آنتیاکسیدانهای طبیعی و مکملهای غذایی مناسب میتوانند مکملهای مهم برای درمان کلاسیک بیماری سلیاک باشند. تحقیقات نشان میدهد که مصرف آنتیاکسیدانی علائم بیماری را کاهش می دهد.
با افزایش مصرف غذاهای غنی از آنتیاکسیدان، سطح سلامت بهبود مییابد. مطالعات نشان دادهاند که انواع توتها، انار، زغال اخته، تمشک، خربزه، توت فرنگی، گیلاس و سیب در میان مواد غذایی بیشترین مقدار آنتیاکسیدانی را دارا میباشند، به طور کلی، رنگ عمیق قرمز یا بنفش، محتوای آنتیاکسیدان بالاتری دارند.
میوههای خشک شده نیز دارای سطح آنتیاکسیدانی بالایی هستند، کشمش، آلو، سبزیجات، لوبیای سیاه، آجیل، چای سبز، قهوه و کاکائو تیره نیز منابع غنی از آنتیاکسیدان به شمار میآیند.
منابع:
Stojiljković, V., Todorović, A., Pejić, S., Kasapović, J., Saičić, Z.S., Radlović, N. and Pajović, S.B., 2009. Antioxidant status and lipid peroxidation in small intestinal mucosa of children with celiac disease. Clinical biochemistry, 42(13), pp.1431-1437.
Stojiljković, V., Pejić, S.A., Kasapović, J., Gavrilović, L., Stojiljković, S., Nikolić, D. and Pajović, S.A.B., 2012. Glutathione redox cycle in small intestinal mucosa and peripheral blood of pediatric celiac disease patients. Anais da Academia Brasileira de Ciencias, 84(1), pp.175-184.
Boda, M. and Nemeth, I., 1992. Decrease in the antioxidant capacity of red blood cells in children with celiac disease. Acta paediatrica Hungarica, 32(3), pp.241-255.