تصور کنید که درد بیش از حد شکمی دارید که اغلب هنگام خوردن یا نوشیدن بدتر میشود و ساعتها ادامه دارد. اینها برخی از نشانههایی است که مردم از پانکراتیت مزمن (CP) رنج میبرند.
داروها ممکن است درد را التیام دهند اما مؤسسه ملی دیابت و بیماریهای گوارشی و كلیوی یادآور میشود که درمان قطعی در موارد دردهای شدید به جز جراحی وجود ندارد. مجله رسمی موسسه انجمن گوارش آمریکا اولین بار است که مکملهای آنتیاکسیدانی را در کاهش درد و کاهش سطح استرس اکسیداتیو در بیماران مبتلا به CP موثر معرفی کرده است.
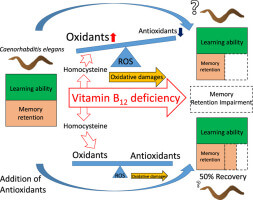
در یک آزمایش بالینی، 127 بیمار مبتلا به CP مورد بررسی قرار گرفتند. افراد گروه دارو یا آنتیاکسیدان دریافت کردند. در پایان شش ماه، افرادی که در گروه آنتیاکسیدان قرار داشتند، روزهای پر از درد ناگهانی را نسبت به گروه دارویی تجربه کردند. افراد مبتلا به پانکراتیت مزمن که آنتیاکسیدانها را مصرف میکردند همچنین قرصهای دارویی کمتری دریافت کردند. علاوه بر این، 32 درصد از بیماران CP که با آنتیاکسیدانها تیمار شدند، درد را آزاد میکردند اما پس از حدود سه ماه از مصرف آنتیاکسیدانها، تسکین درد شروع شد.
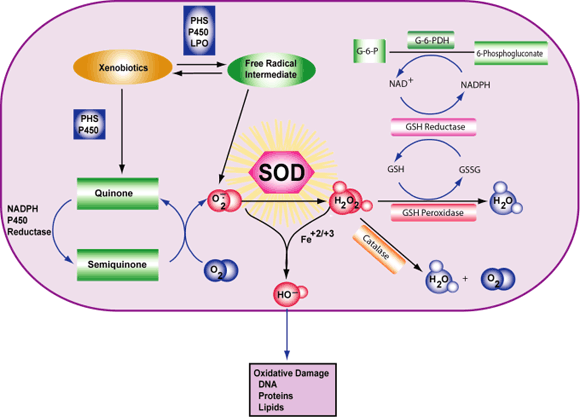
درد شکمی، علائم غالب در بیماران مبتلا به CP، جهت درمان بسیار دشوار است. دلیل اصلی درمان ناکارآمد پزشکی این است که مکانیزم درد در CP به خوبی درک نمیشود. یافتهها پیشرفت قابل توجهی با حضور آنتیاکسیدانها در رابطه با تمام پارامترهای درد در این مطالعه نشان دادهاند. دانشمندان همچنین شاخصهای استرس اکسیداتیو را اندازهگیری کردند و دریافتند که آنها ابتدا افزایش و پس از مکمل آنتیاکسیدانی کاهش مییابند. این مساله نشان میدهد که درمان CP بایستی شامل آسیب رادیکالهای آزاد شود. این امر میتواند در بسیاری از افراد با مصرف مکملهای آنتیاکسیدانی صورت پذیرد.
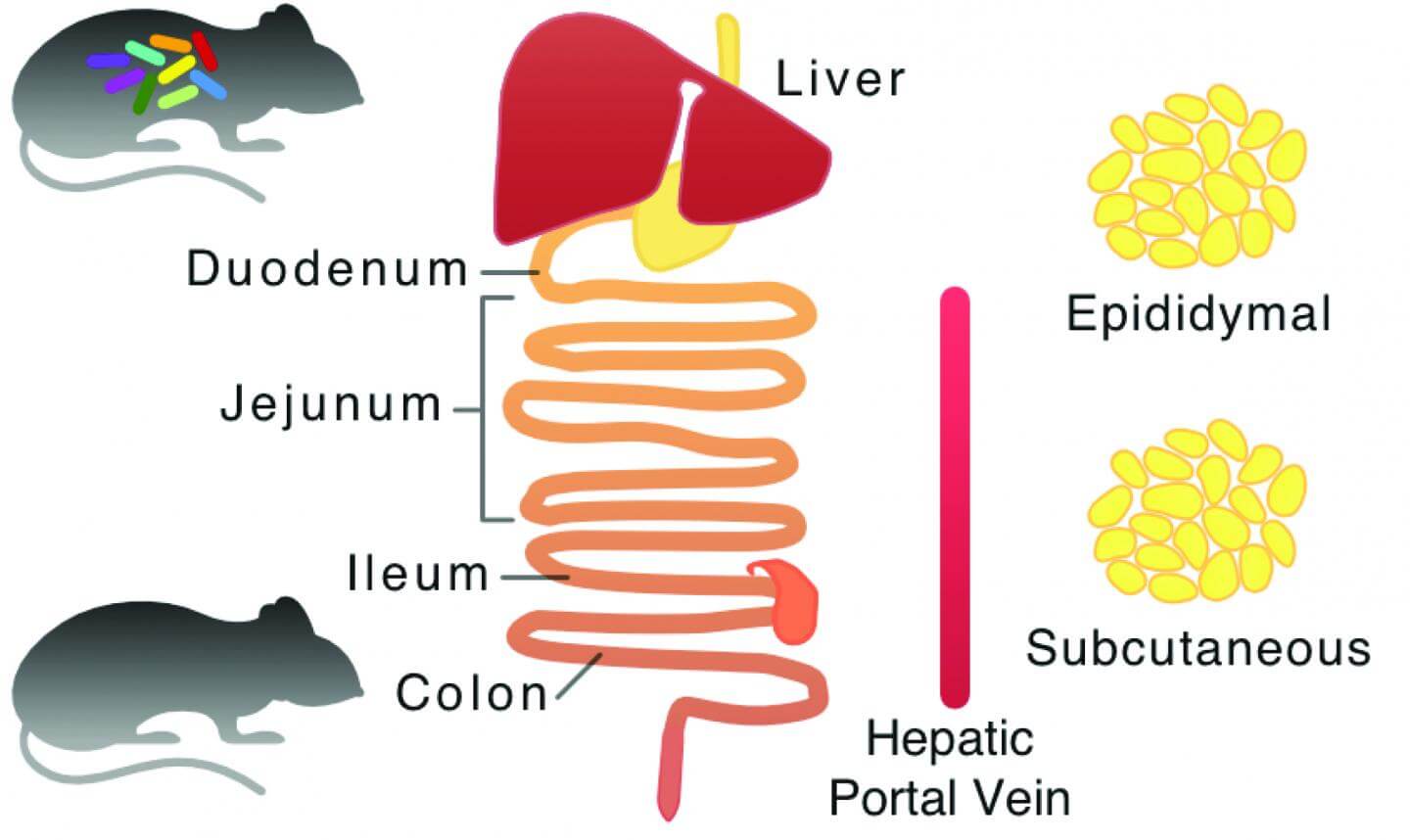
پانکراس غده بزرگی است که در پشت معده قرار دارد و در کنار کیسه صفرا است. آنزیمها و هورمونهای گوارشی، از جمله انسولین و گلوکاگون تولید میکند که به تنظیم قند خون کمک میکنند. پانکراتیت اغلب به عنوان یک حمله ناگهانی آغاز میشود. مصرف الکل و جهشهای ژنتیکی میتوانند باعث ایجاد CP شوند اما گاهی علت آن مشخص نیست. CP یک بیماری التهابی پیشرونده است که میتواند منجر به زخم و از دست دادن عملکرد پانکراس شود. در نتیجه افراد مبتلا به CP میتوانند وزن بیش از حدی از دست بدهند، اسهال مکرر را تجربه کرده و دیابت یا کمبود ویتامین داشته باشند.
منابع:
Bhardwaj, P., Garg, P.K., Maulik, S.K., Saraya, A., Tandon, R.K. and Acharya, S.K., 2009. A randomized controlled trial of antioxidant supplementation for pain relief in patients with chronic pancreatitis. Gastroenterology, 136(1), pp.149-159.
De las Heras, C.G., García, D.L.P.A., Fernandez, M.D. and Fernández, F.J., 2000. Use of antioxidants to treat pain in chronic pancreatitis. Revista espanola de enfermedades digestivas: organo oficial de la Sociedad Espanola de Patologia Digestiva, 92(6), pp.375-385.
Siriwardena, A.K., Mason, J.M., Sheen, A.J., Makin, A.J. and Shah, N.S., 2012. Antioxidant therapy does not reduce pain in patients with chronic pancreatitis: the ANTICIPATE study. Gastroenterology, 143(3), pp.655-663.