طبق یک مطالعه منتشر شده در آوریل و در مجله Science Translational Medicine، دو نوع از داروهای مورد استفاده برای درمان دیابت نوع 2 میتواند متاستاز تومورهای انسان را در موشها گسترش دهد. این دو نوع ترکیب حاوی مهارکنندههای دیپپتیدیل پپتیداز 4 (DPP-4) و بازدارنده آلفالیپوئیکاسید (ALA) است که باعث سرعت بخشیدن به متاستاز ناشی از فعال شدن یک مسیر پاسخ آنتیاکسیدانی میشود. در این مسیر پروتئینهای متاستاز فعال میشوند. نتایج این تیم نشاندهنده ارتباط بین آنتیاکسیدانها و گسترش سرطان است.
مهمترین یافته در این زمینه بیان میکند که متاستاز، سرطانهای موجود را با فعال شدن پاسخ آنتیاکسیدانی ترویج میدهد.
زاکاری شافر، زیستشناس سلولی از دانشگاه نوتردام، گفت: “این اطلاعات محرمانه هستند و نتیجه تحقیق با مطالعات دیگر مطابقت دارد که فعالیت آنتیاکسیدانی میتواند برای متاستاز سلولهای سرطانی مفید باشد.”
ژنگ و همکاران برای اولین بار از داروهای ضد دیابتی معمول استفاده کردند، از جمله متفورمین و آنالوگهای انسولین وتوانایی آنها را برای افزایش تکثیر یا افزایش مهاجرت سلولهای سرطانی در آزمایشگاه بررسی کردند. محققان نشان دادند که مهارکنندههای DPP-4 از مهاجرت و تهاجم سلولها جلوگیری میکند اما بر روی تکثیر سلولهای سرطانی ملانوم، کبد، کولون، پستان، ریه و تخمدان تاثیرگذار نیست.
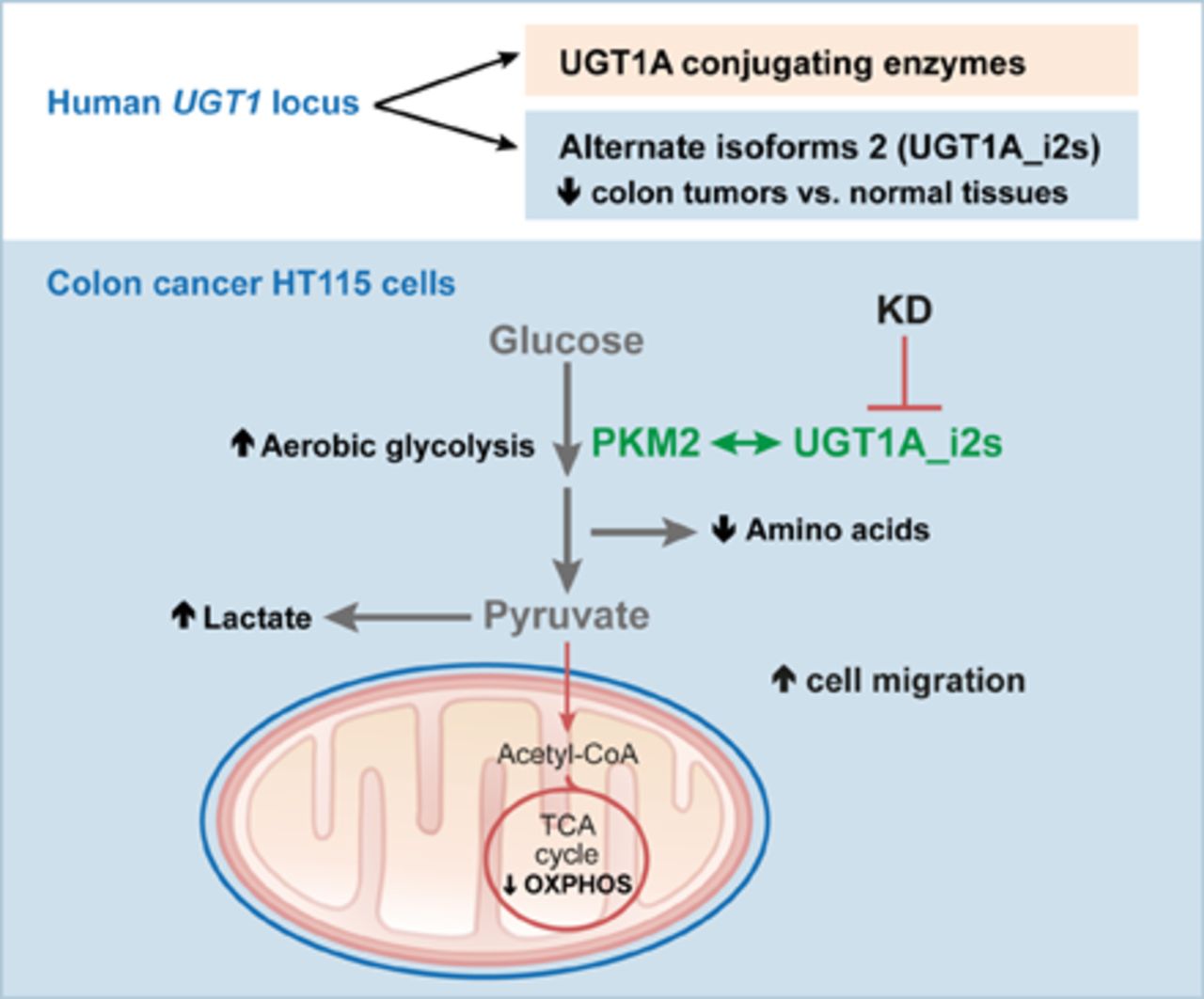
در موشها، این داروها موجب انتشار بیشتر سلولهای تومور کبدی و کولون و همچنین افزایش میکرومتاستاز در مقایسه با حیوانات با همان تومورهایی بود که هیچ داروهای ضددردی دریافت نکردند. آزمایشهای بیشتر در آزمایشگاه نشان داد که اثرات مهارکننده DPP-4 بر روی انتقال تومور سلول با توانایی ترکیبات برای کاهش استرساکسیداتیو سلولهای سرطانی همراه است: داروها منجر به کاهش گونههای فعال اکسیژن (ROS) ، افزایش گلوتاتیون و افزایش آنتیاکسیدان آندوژنز میشود. محققان نشان میدهند که مهارکننده سنتز گلوتاتیون در سلولهای سرطانی علاوه بر مهارکردن DPP-4 مانع از انتقال سلولهای تومور میشود.
برای درک اینکه چگونه این ترکیبات بر روی مسیرهای استرس اکسیداتیو سلولی اثر میگذارند، محققان فاکتور رونویسی (NRF2) را که از طریق بازدارنده DPP-4 فعال میشوند، هم در کشت سلولی و هم در موش بررسی کردند.. پنج مهارکننده متفاوت DPP-4 همه در NRF2 فعال شدهاند. هنگامی که محققان NRF2 را در پروتئین بازدارنده DPP-4 و سلولهای سرطانی کبد از بین بردند، سلولها کاهش مهاجرت سلولهای تومور و بیان پروتئینهای مرتبط با متاستاز را نشان دادند.
محققان اثر مشابهی را در in vivo مشاهده کردند. موشهایی که با سلولهای نابودکننده NRF2 تلقیح شده بودند، متاستازهای ناشی از مهارکننده DPP-4 کمتری داشتند. محققان گزارش دادند که NRF2 همچنین متاستازهای مستقل از هرگونه درمان دارویی دیابت را تحت تاثیر قرار داده است. فعالسازی فاکتور رونویسی باعث بیان پروتئینهای متاستاز و مهاجرت سلولی در کشت شده و فعالسازی فارماکولوژیک NRF2 در موش، باعث افزایش میکرومتاستاز شد.
یکی دیگر از فعال کننده NRF2 شناخته شده، با نام ALA که برای درمان نوروپاتی دیابتی استفاده میشود، و اثرات مشابهی را به عنوان مهارکننده DPP-4 دارد، مورد مطالعه قرار گرفت. تجزیه و تحلیل دادههای بیان اولیه تومور و متاستاتیک، نشان داد که در نمونههای با متاستاتیک بیشتر، احتمال افزایش بیان NRF2 را با متاستاز گره لنفاوی مرتبط میکند. مطالعات قبلی نشان داده است که NRF2 توسط آنکوژنها فعال میشود، که تومورها را قادر میسازد تا ROS را خنثی کنند که مانع رشد آنها میشود. شافر اشاره کرد که آیا سایر داروها با فعالیت آنتیاکسیدانی با یک مکانیزم مشابه کار میکنند یا اینکه سلولهای سرطانی، خود نیز از مکانیسمهای دیگر برای حفظ آنتیاکسیدان استفاده میکنند.
گام بعدی این است که مطالعه متاستاز تومور در موشهای دیابتی داشته باشیم، که به اندازه کافی منعکسکننده کاربرد بالینی فعلی داروهای ضدویروسی خواهد بود.
برگئو تأکید کرد: “آنتی اکسیدانها و داروهایی که NRF2 را فعال میکنند باعث ایجاد سرطان نمیشوند.” “در عوض، آنها به سلولهای سالم کمک میکنند سالم بمانند و به سلولهای سرطانی کمک می کنند تا در بدن گسترش پیدا کنند.
منابع:
Caglayan, A., Katlan, D.C., Tuncer, Z.S. and Yüce, K., 2019. Evaluation of trace elements associated with antioxidant enzymes in blood of primary epithelial ovarian cancer patients. Journal of Trace Elements in Medicine and Biology, 52, pp.254-262.
Shrivastava, A., Aggarwal, L.M., Mishra, S.P., Khanna, H.D., Shahi, U.P. and Pradhan, S., 2019. Free radicals and antioxidants in normal versus cancerous cells—An overview.