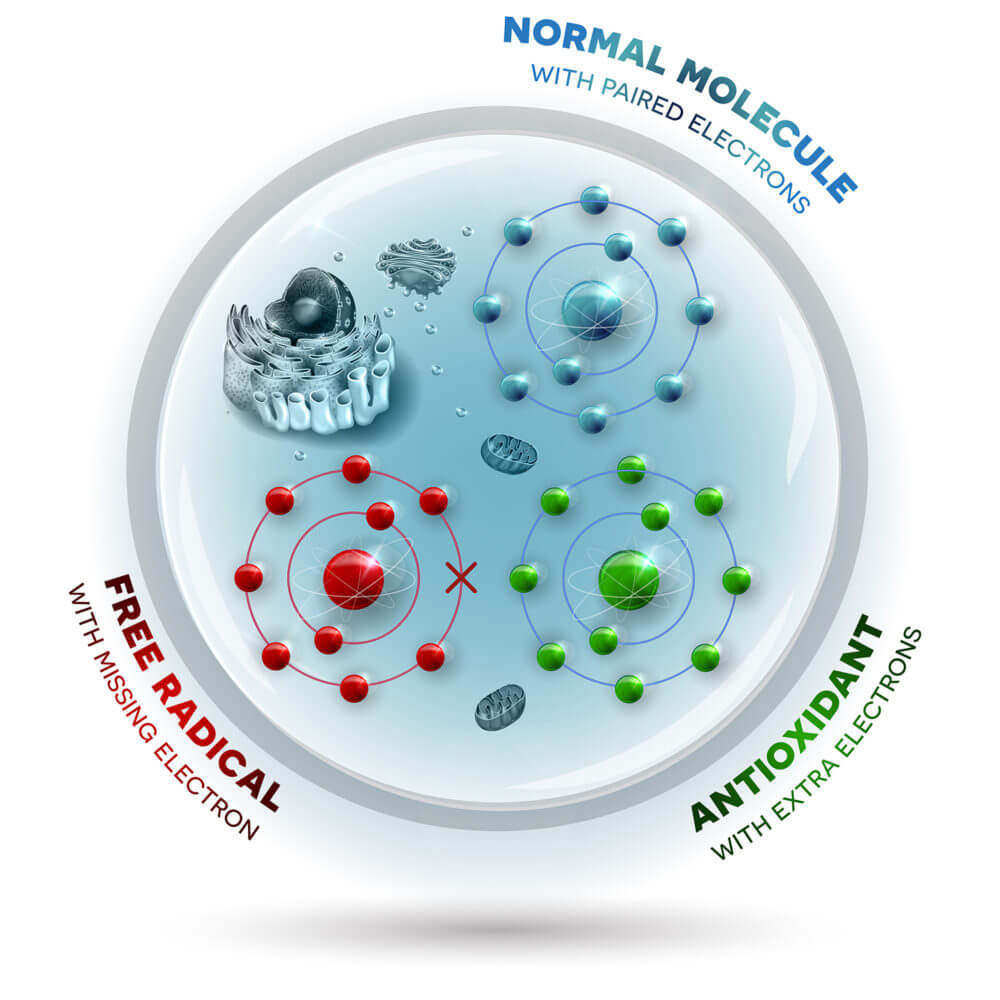
رادیکالهای آزاد تولید شده توسط میتوکندری سلول – اندامک تولید انرژی در سلول – در واقع برای بهبود زخم مفید هستند.
بررسی محققان نشان میدهد گونههای فعال اکسیژن مولکولهای واکنشی شیمیایی حاوی اکسیژن هستند مانند پراکسیدها که معمولا به عنوان رادیکالهای آزاد نامیده میشوند و برای درمان زخمهای پوستی مناسب میباشند. محققان دریافتند که رادیکالهای آزاد تولید شده در میتوکندری نه تنها برای التیام زخمهای پوست ضروری است، بلکه افزایش سطوح گونه فعال اکسیژن یا ROS در واقع میتواند باعث بهبودی سریعتر زخم شود.
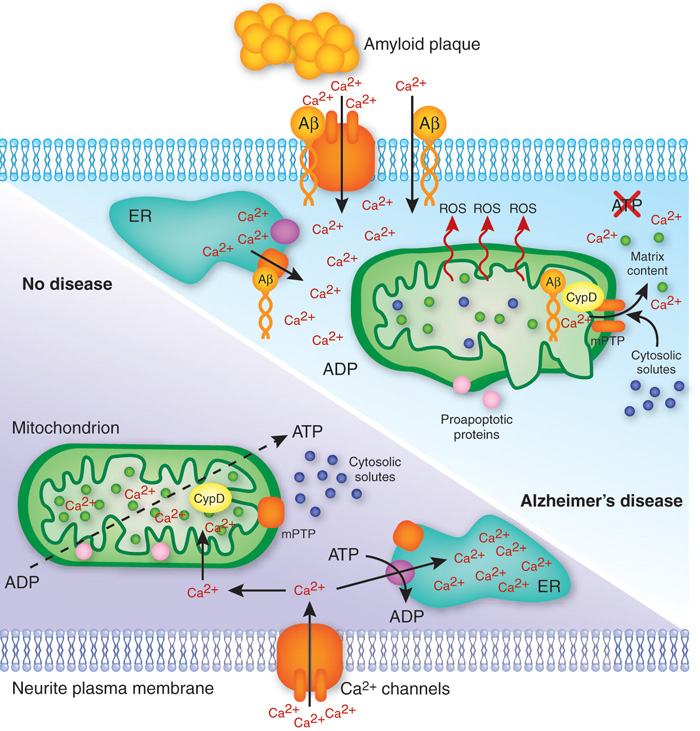
ROS از مسیرهای مختلفی در سلول تولید میشود اما جزئیات فرایند تولید در میتوکندری مشخص نشده است. اما بیان شده است که میتوکندریها نقش به سزایی در بهبود زخم دارند.
رادیکالهای آزاد یا ROS، به مدت طولانی شناخته شدهاند و به DNA، RNA و پروتئینها آسیب میرسانند. از آنجا که چنین آسیبهای اکسیداتیو به پیری زودرس و سرطان کمک میکند، بسیاری از مردم آنتیاکسیدانها را برای کاهش آسیب سلولی از رادیکالهای آزاد مصرف میکنند.
اما محققان دریافتند در حالی که ROS بیش از حد در سلول ممکن است برای اندام مضر باشد، از بین بردن ROS به طور کلی مانع بهبود زخم میشود. کشف دانشمندان به دنبال توسعه داروهای جدید برای درمان سالمندان و افراد مبتلا به دیابت است که ارتباط تنگاتنگی با بهبود زخم دارند. به نظر می رسد بدن انسان نیاز به یک سطح بهینه از سیگنالهای ROS دارد. سطح بیشتر یا کمتر از مقدار بهینه برای بدن مضر است. طراحی ژنهایی که ROS را در میتوکندری تولید کرده و آنتیاکسیدانها را در سطح بهینه از بین برده بودند، باعث بهبود زخم و تسریع در روند التیام زخم شدند.
این آزمایشات مراحل آزمایشگاهی خود را طی میکنند اما دانشمندان معتقدند این مسیرهای ژنتیکی حفظ شدهاند، به طوری که در مهره داران و پستانداران نیز با همین مکانیسم عمل میکنند.
Altavilla, D., Saitta, A., Cucinotta, D., Galeano, M., Deodato, B., Colonna, M., Torre, V., Russo, G., Sardella, A., Urna, G. and Campo, G.M., 2001. Inhibition of lipid peroxidation restores impaired vascular endothelial growth factor expression and stimulates wound healing and angiogenesis in the genetically diabetic mouse. Diabetes, 50(3), pp.667-674.
Valko, M., Leibfritz, D., Moncol, J., Cronin, M.T., Mazur, M. and Telser, J., 2007. Free radicals and antioxidants in normal physiological functions and human disease. The international journal of biochemistry & cell biology, 39(1), pp.44-84.